Разряд заряд аккумулятора
Режимы разряда и заряда автомобильных аккумуляторов.
В процессе длительного (несколько месяцев) хранения автомобильных аккумуляторных батарей происходит их саморазряд, в связи с чем рекомендуется не реже одного раза в месяц производить подзарядку аккумуляторов. Однако обычная подзарядка не в состоянии предотвратить сульфатацию пластин, приводящую к уменьшению емкости аккумулятора и снижению срока его службы. Для того чтобы исключить эти нежелательные явления, рекомендуется время от времени производить тренировку аккумулятора:
разрядку его током, в амперах численно равным 1/20 номинальной емкости, выраженной в ампер-часах, до напряжения 10,5 В, и последующую зарядку до напряжения 14,2...14,5 В. Такой зарядно-разрядный цикл можно повторять неоднократно, если батарея сильно засульфатирована или длительное время находилась в полуразряженном состоянии.
Для этой цели требуется зарядно-разрядное устройство
- производить разрядку аккумулятора до напряжения 10,5 В;
- автоматически начинать зарядку по окончании разрядки;
- вести зарядку асимметричным током при соотношении зарядной и разрядной составляющих равном 10;
- прекратить зарядку аккумулятора при достижении напряжением на зажимах аккумулятора значения
14,2...14,5 В, что соответствует сообщению аккумулятору его полной номинальной емкости;
- контроль напряжения происходит в момент, когда зарядный ток через аккумулятор не протекает;
- прекратить разрядку аккумулятора при пропадании сетевого напряжения;
1. При зарядке аккумулятора постоянным, не изменяющимся в процессе зарядки током ее прекращают вручную по истечении определенного времени. На такой режим ориентированы многие наиболее дешевые зарядные устройства. Зарядный ток в них составляет обычно I=0,1·Е, где I - зарядный ток в амперах, а Е - емкость аккумулятора в амперчасах. В этом режиме емкостной КПД аккумулятора принимают равным 2/3 и, соответственно, длительность зарядки устанавливают равной 15 часам. Режим зарядки малым током (он может быть и меньше 0,1·Е при соответствующем увеличении продолжительности зарядки) замечателен тем, что даже при значительной перезарядке аккумулятор не будет поврежден, во всяком случае - не взорвется :).
2. Аккумулятор заряжают постоянным током, многократно превышающим 0,1·Е (в 10...20 раз). Зарядка прекращается автоматически по истечении заданного - более короткого - времени. В режиме такой интенсивной зарядки обязательно должно соблюдаться следующее. Во-первых, аккумулятор необходимо предварительно разрядить (обычно - до 1В на банку); во-вторых, должна быть обеспечена строгая зависимость продолжительности зарядки от установленного значения зарядного тока и, в третьих, обеспечено аварийное его отключение (например, по перегреву корпуса).
По идее к этой категории относятся многие зарядные устройства, появившиеся на нашем рынке, но, к сожалению, далеко не все они обеспечивают должную безопасность.
3. Ток зарядки - не обязательно постоянный. Зарядку аккумулятора прекращают при увеличении его температуры. Этот способ имеет серьезные недостатки (аккумулятор почти всегда перезаряжается, ненадежен тепловой контакт и др.) и используется, как правило, лишь для аварийного отключения аккумулятора.
4. Ток зарядки - фиксированный, многократно, как правило, превышающий 0,1·Е. По достижении на аккумуляторе заданного напряжения зарядка заканчивается автоматически. Этот принцип долгое время использовался в самых лучших зарядных устройствах, потеснив систему зарядки аккумулятора малым током. Установка порогового напряжения здесь весьма критична. Обычно его значение выбирают в пределах 1,45...1,55В на аккумуляторную банку, чаще - 1,48В. Пороговое напряжение зависит, к тому же, от температуры окружающей среды и «возраста» аккумулятора. Неизменный ток зарядки здесь, вообще говоря, не обязателен. Но это упрощает учет потерь на подводящих проводах. Если из-за их неучета на аккумуляторе будет установлено заниженное пороговое напряжение, это обернется недобором заряда, а установленное лишь на один милливольт выше реального, приведет к тому, что процесс зарядки аккумулятора никогда не кончится. Вернее, кончится тем, что аккумулятор либо перегреется - при малом зарядном токе, либо взорвется - при большом.
Во избежание этого некоторые зарядные устройства по достижении напряжения, чуть меньше порогового, переходят на дозарядку аккумулятора безопасным током, которым ее и завершают.
5. Процесс зарядки контролируют по скорости увеличения напряжения на аккумуляторе: оно быстро увеличивается непосредственно перед ее завершением. Отследив этот момент, зарядное устройство уменьшает большой ток зарядки (он доходит в них до 2·Е) до малого, безопасного, которым зарядка и завершается. По причинам, изложенным в п.4, оба эти тока также лучше иметь фиксированными, не изменяющимися во времени. Этот способ стал привлекать к себе внимание с появлением специализированной микросхемы U2402B.
6. Как и в предыдущем случае, при зарядке постоянным током состояние аккумулятора определяют по скачку напряжения. Для получения хороших характеристик зарядку ведут током не менее 2·Е.
7. А вот теперь рассмотрим случай глубокого разряда: заряжать АКБ в этом случае надо пониженным напряжением (12В..13В). Кислота из электролита ушла в пластины, если дать номинальный зарядный ток, начнется процесс электролиза воды. Надо следить за тем, чтобы ток в начале заряда не превысил 1/20 ее емкости в Ампер*часах (в принципе, это должно произойти автоматически, в отличие от ситуации, когда сразу на клеммы подают 14,4 В). Будет больше - снижайте напряжение. Понемногу ток будет расти - это нормально. Это кислота вылезает из глубины пластин наружу, сульфат свинца даёт приток кислоты, плотность электролита повышается. Когда ток поднимется до 1/10 емкости АКБ, или даже больше, а совсем хорошо - когда он после этого подъема даже начнет снижаться - тогда можно переходить на описанный выше процесс заряда, т.е. ставить напряжение 14,4В.
8. Зарядные устройства
К наиболее интересным можно отнести сегодня зарядное устройство ULTRA DUO, в котором зарядка заканчивается по всплеску напряжения на аккумуляторе.
В зарядном устройстве MULTI-CHARGE-A-MATIC CG-325 фирмы HITEC окончание зарядки определяется как ив предыдущем случае, но зарядка ведется установленным постоянным током (максимально 4,5А). Кроме таких обычных функций, как разрядка аккумулятора перед зарядкой, проверка его емкости, защита от переполюсовки, контроль длительности зарядки и звуковая сигнализация ее окончания, это устройство благодаря встроенному преобразователю напряжения может заряжать от 12-вольтного автомобильного аккумулятора десять последовательно соединенных никель-кадмиевых аккумуляторов (напряжение на которых в заряженном состоянии доходит до 16В). Это оценят, прежде всего, автомобилисты, пользующиеся портативными радиостанциями.
По установившейся терминологии зарядка аккумулятора может быть очень быстрой (до 15мин), быстрой (до 1ч), ускоренной (до 3...4ч), нормальной (от 12 до 16ч) и медленной. Реальная емкость аккумулятора зависит от температуры и значений тока зарядки и разрядки. Наибольшая измеренная емкость получается при зарядке аккумулятора большим током и разрядке малым.
Теперь мне стало ясно, что конструкторы автомобилей были тысячу раз правы, используя на них обычные электроаккумуляторы, а не конденсаторы или сверхпроводящие магниты.
Действительно, автомобильные аккумуляторы могут месяцами хранить энергию, причем в достаточно большом количестве.
9. Из истории
История электроаккумуляторов берет начало со знаменитого опыта, проделанного итальянским физиком Алессандро Вольтой в 1799 году. Ученый опустил медный и цинковый электроды в разбавленную серную кислоту и обнаружил, что между электродами возникла разность потенциалов. Соединив электроды проводником – проволочкой, Вольта получил в ней электрический ток. Тем самым он доказал, что различные металлы, помещенные в растворы кислот, образуют источник тока.
Это был первый в мире гальванический элемент, названный так потом в честь итальянского физика и врача Луиджи Гальвани, который еще до Вольты заметил появление тока при взаимодействии двух разных металлов в проводящей жидкости – электролите.
Правда, есть сведения, что гальванические элементы существовали и в древности. Во время археологических раскопок были найдены глиняные кувшины с напоминающими электроды цилиндрами из разных металлов, причем некоторые ученые считают, что электролитом тогда служили вино или уксус. И будто бы с помощью этих элементов древние мастера умели делать гальванические покрытия: например, наносили тончайшую пленку золота на украшения.
Так или иначе, огромная заслуга Вольты в том, что он не только построил гальванический элемент, но и объяснил его действие, чего по вполне понятным причинам не могли сделать древние.
Элемент Вольты давал очень маленькое напряжение. Чтобы повысить его, стали изготавливать батареи из медных и цинковых пластин, переложенных прокладками, смоченными серной кислотой. Батареи эти, названные вольтовыми столбами, обеспечивали уже достаточно большое напряжение. После Вольты немало ученых – Лекланше, Грене, Даниэль, Грове и другие – разрабатывали свои, все более и более совершенные гальванические элементы. Элемент Лекланше, например, послужил прообразом современных «сухих» батарей, используемых для питания карманных фонариков, радиоприемников, электрифицированных игрушек и прочих устройств. Электроды таких батарей, как когда-то у Лекланше, твердые – цинковый стаканчик и графитовый стержень. А вот электролит уже не жидкий. Ведь жидкость может в любой момент пролиться, а делать элемент герметичным дорого и сложно. Вот и заменили жидкость желеобразным электролитом. Получился удобный и практичный источник электричества.
Свинцово-кислотные аккумуляторы весьма экономичны, однако они и капризны, часто портятся, недолговечны. К тому же свинец – сравнительно редкий и дорогой металл, а кислота – опасна в обращении. Естественно, что ученые стали искать новые материалы и новые принципы работы аккумуляторов. Так возник второй основной тип электрохимических аккумуляторов – щелочные аккумуляторы. Создание их тесно связано с именем знаменитого американского ученого и изобретателя Томаса Эдисона.
В этих аккумуляторах электролитом служит уже не кислота, а щелочь – 20-процентный раствор едкого кали. Пластины изготовлены из стальных решеток с карманами в них. У положительных пластин карманы заполнены смесью, содержащей окись никеля, а у отрицательных – губчатым кадмием. Корпус щелочного аккумулятора стальной, что придает устройству большую прочность.
Щелочные аккумуляторы дороже кислотных и менее экономичны. Но, несмотря на это, положительные их качества преобладают – они неприхотливы, прочны, долговечны. Поэтому они все больше входят в технику. Например, на троллейбусах применяются именно такие накопители. Их можно видеть в транзисторных приемниках, телефонных и слуховых аппаратах, карманных фонариках и в других устройствах. Во многих радиоприборах присутствуют миниатюрные аккумуляторы, тоже щелочные, под названием «кнопочные», так как они внешне напоминают кнопку. Ценность их в том, что они герметично закрыты, совершенно нечувствительны к перезарядку и переразрядку, не требуют ухода. Обычные крупные аккумуляторы этим «похвастать» не могут.
На некоторых спутниках связи и космических станциях применяются очень дорогие, но зато великолепные по своим характеристикам серебряно-цинковые щелочные аккумуляторы. Им нипочем ни большие токи, ни низкие, до минус 60 градусов, температуры. Плотность энергии, накапливаемой в них, в пять раз выше, чем у кислотных аккумуляторов, а плотность мощности – вдвое выше.
Всем хороши серебряно-цинковые аккумуляторы, хоть сейчас ставь их на автомобиль. Масса аккумулятора для прохождения стокилометрового пути не превысит ста килограммов...
Чтобы аккумулятор мог стать поистине массовым и перспективным, он должен содержать материалы, которых на Земле вдоволь.
Сейчас ученые связывают свои надежды с необычным на первый взгляд аккумулятором, в котором используются гальванические пары «сера – натрий» и «хлор – литий». Металлы – натрий или литий – там расплавлены, их температура достигает нескольких сот градусов. Расплавленный натрий соединяется в аккумуляторе с горячей жидкой серой, а литий взаимодействует с раскаленным газом – хлором. Из-за того, что содержимое таких аккумуляторов при работе нагрето до 300...800 градусов, они получили название горячих.
Мне происходящее внутри горячих аккумуляторов почему-то сразу напомнило мифологический ад, о котором я в детстве немало начитался. Достаточно было представить расплавленную серу, в которой «варится» расплавленный же натрий, тот самый натрий, что и от воды-то загорается и даже взрывается! О хлоре и говорить нечего – это один из наиболее ядовитых газов, чрезвычайно активный даже при комнатной температуре, а что будет при восьмистах градусах! Недаром ученые, который уж год бьются над созданием корпуса к этому «адскому» накопителю – мало какой материал выдерживает такую начинку.
Однако к чести горячих аккумуляторов, они при низкой своей стоимости развивают плотность энергии раз в десять большую, чем свинцово-кислотные аккумуляторы, и плотность мощности у них значительно выше. Если свинцово-кислотные аккумуляторы накапливают в килограмме своей массы 64 килоджоуля энергии, а щелочные – 110, то горячие серно-натриевые – 400...700 килоджоулей!
Автомобилю для пробега в 100 километров хватило бы всего 50 килограммов серно-натриевого аккумулятора. 150 килограммов на 300 километров пробега – это неплохие результаты. Но... горячие аккумуляторы перед началом работы надо разогревать, оболочка их не выдерживает долго «адское» содержимое. Да и при аварии машины с этим аккумулятором присутствовать даже зрителем никому не пожелаешь.
Более спокойный «характер» у новых, медно-литиевых аккумуляторов. Они имеют катод из медного сплава и анод из пористого лития. Электролит органический, с высокой электропроводностью. Плотность энергии в опытных образцах этих аккумуляторов в полтора раза выше, чем у серебряно-цинковых, но, что самое важное, у них возможно получение высоких удельных мощностей. Если же вместо меди взять фтористое соединение никеля, то и процесс зарядки аккумулятора можно сильно сократить, всего до нескольких минут, что также очень существенно.
Интересны аккумуляторы на основе цинка и... обыкновенного воздуха. Цинковый анод здесь просто окисляется кислородом воздуха, поэтому весь запас энергии в батарее обусловлен только количеством цинка. Катод изготовлен из пористого никеля и почти не расходуется, а анод по мере износа заменяется новым или восстанавливается пропусканием зарядного тока.
Своеобразие этих батарей заключается в том, что они могут работать как в режиме аккумуляторов, так и в режиме обычных гальванических элементов, попросту «сжигая» цинк в кислороде воздуха. Именно в этом случае цинковые аноды приходится заменять, но плотность энергии элемента при этом получается почти вдвое большей, чем у аккумулятора.
Однако как ни хороши описанные выше аккумуляторы-рекордсмены, специалисты все-таки считают, что проблему создания современного электромобиля с дальностью пробега 120...150 километров должны решить не они, а дешевые и недефицитные никель-цинковые аккумуляторы. По плотности энергии и мощности такие аккумуляторы находятся между обычными и серебряно-цинковыми аккумуляторами. Возникли они в результате замены у серебряно-цинковых элементов дорогого серебра на сравнительно дешевый никель. Новые, рулонные, типы аккумуляторов
Технология производства рулонных элементов позволяет аккумуляторам типа Optima совмещать в себе преимущества стартерных и тяговых аккумуляторов. Аккумуляторы Optima многократно выдерживает циклы разряда.заряда без ущерба емкости и идеален для сезонного применения, так как имеет низкую степень саморазряда. Все модели аккумуляторов не требуют обслуживания, имеют прочный герметичный корпус. Могут работать в любом положении без вытекания электролита.
Аккумуляторы Optima различаются цветовой маркировкой верха аккумулятора. Минимальную. емкость имеют аккумуляторы с красным верхом RT (56 А/ч, 830 ампер, 12 В, 17.7 кг, 245х172х199 мм 12 тыс. стартовых циклов) применяются в качестве стартерных, удобны при частых пусках двигателя. Аккумуляторы с желтым верхом YT (60 А/ч, 750 А, 12В, 19,5 кг, 245х172х199 мм) применяются на транспортных средствах оснащенных дополнительными мощными потребителями электроэнергии - лебедки, усилители, подогреватели двигателей. Поддерживает достаточно высокое напряжение при длительных разрядных токах в значительно большей степени, чем ток обычного аккумулятора. Аккумуляторы ВТ (Blye Top) совмещает в себе качества стартерного и тягового аккумуляторов. Емкость синего аккумулятора 75 А/ч, габариты 254х172х199
Аккумулятор собран из рулонных элементов. Элемент представляет собой рулон, между слоями химически чистого свинца, свернутого в рулон, проложено микропористое волокно, припитанное электролитом. Характеристики аккумуляторов Optima сохраняют свои характеристики в диапазоне от -60 до +80 градусов С. Долговечность аккумуляторов в 4 раза больше чем у обычных аккумуляторов.
Емкость батареи Optima в начальный период эксплуатации составляет примерно 85% от номинала. В процессе работы после 17-19 циклов разрядки/зарядки емкость достигает номинальной. Для подготовки аккумулятора к работе предлагается провести циклирование (тренировка) аккумулятора в соответствии со следующими рекомендациями:
1. Разрядить полностью заряженную батарею до напряжения 10.5В
2. Зарядить аккумулятор в течение 16 часов током 4А.
3. Повторить операции п.1 и п.2 три раза.
Существует несколько режимов заряда тяговых батарей типа Optima. Это батареи с желтым и синим верхом. Ниже приведены способы заряда.
1.На автомобиле при постоянном напряжении от генератора 14.2 - 15.0 В.
2. От зарядного устройства при постоянном напряжении. Напряжение 14.2-15.0 В, ток 10А. Продолжительность заряда до момента, когда ток упадет ниже 0.2А
3. При использовании аккумулятора в качестве тягового следует его заряжать в три ступени:
- 1 ступень: заряжать током 25А до достижения напряжения 14.7В
- 2 ступень: продолжать зарядку при фиксированном напряжении 14.7 до тех пор пока ток заряда не снизится до значения менее 1А.
- 3 ступень: Поднять ток заряда до 2А и заряжать в течение 1 часа. Напряжение не имеет значения.
4. Существует методика ускоренного заряда. Заряд напряжением 15.6 В без ограничения зарядного тока. Контролировать температуру корпуса батареи. Температура не должна превышать 50 градусов. Продолжительность определяется опытным путем, чтобы обеспечивалась зарядка 110-120% от использованной емкости (обращаю внимание - не номинальной).
5. Стационарное использование (флотирующая зарядка). При работе в буферном питании или при хранении. Заряд напряжением от 13.2 до 13.6В током 120 миллиампер. Похожие материалы: Источник:
1.4. Основные технические характеристики акб. Напряжение аккумулятора при заряде и разряде
Разность потенциалов на полюсных выводах аккумулятора(батареи) в процессе заряда или разряда при наличии тока во внешней цепи принято называть напряжением аккумулятора (батареи). Наличие внутреннего сопротивления аккумулятора приводит к тому, что его напряжение при разряде всегда меньше ЭДС, а при заряде – всегда больше ЭДС.
При заряде аккумулятора на его выводах напряжение должно быть больше его ЭДС на сумму внутренних потерь.
В начале заряда происходит скачок на величину напряжения омических потерь внутри аккумулятора, а затем резкое повышение за счет напряжения потенциала поляризации, вызванное в основном быстрым увеличением плотности электролита в порах активной массы. Далее происходит медленный рост напряжения, обусловленный главным образом ростом ЭДС аккумулятора вследствие увеличения плотности электролита.
После того, как основное количество сульфата свинца преобразуется в РЬО2 и РЬ, затраты энергии все в большей мере вызывают разложение воды (электролиз) Избыточное количество ионов водорода и кислорода, появляющееся в электролите, еще больше увеличивает разность потенциалов разноименных электродов. Это приводит к быстрому росту зарядного напряжения, вызывающему ускорение процесса разложения воды. Образующиеся при этом ионы водорода и кислорода не вступают во взаимодействие с активными материалами. Они рекомбинируют в нейтральные молекулы и выделяются из электролита в виде пузырьков газа (на положительном электроде выделяется кислород, на отрицательном – водород), вызывая «кипение» электролита.
Если продолжить процесс заряда, можно увидеть, что рост плотности электролита и зарядного напряжение практически прекращается, так как уже почти весь сульфат свинца прореагировал, и вся подводимая к аккумулятору энергия теперь расходуется только на протекание побочного процесса – электролитическое разложение воды. Этим объясняется и постоянство зарядного напряжения, которое служит одним из признаков окончания зарядного процесса.
После прекращения заряда, то есть отключения внешнего источника напряжения на выводах аккумулятора резко снижается до значения его неравновесной ЭДС, или на величину омических внутренних потерь. Затем происходит постепенное снижение ЭДС (вследствие уменьшения плотности электролита в порах активной массы), которое продолжается до полного выравнивания концентрации электролита в объеме аккумулятора и порах активной массы, что соответствует установлению равновесной ЭДС.
При разряде напряжение аккумулятора на его выводах меньше ЭДС на величину внутреннего падения напряжения.
В начале разряда напряжение резко падает на величину омических потерь и поляризации, обусловленной снижением концентрации электролита в порах активной массы, то есть концентрационной поляризации. Далее при установившемся (стационарном) процессе разряда происходит снижение плотности электролита в объеме аккумулятора, обусловливающее постепенное снижение разрядного напряжения. Одновременно происходит изменение соотношения содержания сульфата свинца в активной массе, что также вызывает повышение омических потерь. При этом частицы сульфата свинца (имеющего примерно втрое больший объем в сравнении с частицами свинца и его двуокиси, из которых они образовались) закрывают поры активной массы, чем препятствуют прохождению электролита в глубину электродов.
Это вызывает усиление концентрационной поляризации, приводящее к более быстрому снижению разрядного напряжения.
При прекращении разряда напряжение на выводах аккумулятора быстро повышается на величину омических потерь, достигая значения неравновесной ЭДС. Дальнейшее изменение ЭДС вследствие выравнивания концентрации электролита в порах активных масс и в объеме аккумулятора приводит к постепенному установлению значения равновесной ЭДС.
Напряжение аккумулятора при его разряде определяется в основном температурой электролита и силой разрядного тока. Как сказано выше, сопротивление свинцового аккумулятора (батареи) незначительно и в заряженном состоянии составляет всего несколько миллиОм. Однако при токах стартерного разряда, сила которых в 4–7 раз превышает значение номинальной емкости, внутреннее падение напряжения оказывает существенное влияние на разрядное напряжение. Увеличение омических потерь с понижением температуры связано с ростом сопротивления электролита. Кроме того, резко возрастает вязкость электролита, что затрудняет процесс диффузии его в поры активной массы и повышает концентрационную поляризацию (то есть увеличивает потери напряжения внутри аккумулятора за счет снижения концентрации электролита в порах электродов).
При токе более 60 А зависимость напряжения разряда от силы тока является практически линейной при всех температурах.
Среднее значение напряжения аккумулятора при заряде и разряде определяют как среднее арифметическое значений напряжения, измеренных через равные промежутки времени.
Электрическая емкость
Электрическая емкость – характеризует количество электричества, которое способна отдать аккумуляторная батарея при длительном режиме разряда. Электрическая емкость батареи определяется либо при 20‑часовом разряде, либо в режиме резервной емкости.
Номинальная электрическая емкость Cn – емкость 20‑часового разряда аккумуляторной батареи. Именно ее пока регламентируют в большинстве нормативных документов европейских производителей, в российском ГОСТ 959–2002, вступившем в действие с июля 2003 года, и указывают на этикетке аккумуляторной батареи. номинальной разрядной емкостью С20, гарантируемой фирмой изготовителем, считается емкость 20 часового режима разряда. Разряд батарей при испытании на емкость 20 часового режима разряда проводят то ком IP = 0,05*С20 при температуре +25°С до конечного разрядного напряжения 10,5 В у 12‑ти вольтной батареи (1,75 В на аккумулятор). Например, для аккумуляторной батареи емкостью 60 А/ч ток разряда составляет 3 А, а для аккумулятора, емкостью 90 А/ч – 4,5 А. При определении номинальной емкости разряд прекращается при напряжении 10,5 В на 12‑вольтовой батарее.
Резервная емкость(Rc) – это запас емкости аккумулятора, измеренный в минутах при разряде током в 25 А для батарей любой емкости при температуре 27°С. Она приблизительно соответствует времени движения автомобиля при выходе из строя его генератора. Для аккумулятора номинальной емкостью 55 А/ч резервная емкость составляет 85–90 мин. Это значит, что при выходе из строя генератора, автомобиль сможет двигаться еще примерно 1,5 часа за счет энергии аккумулятора, полностью заряженной на момент поломки. Приблизительно Rc = 1,63 Сn.
Внутреннее сопротивление аккумулятора
Сопротивление, оказываемое аккумулятором протекающему внутри него току (зарядному или разрядному), принято называть внутренним сопротивлением аккумулятора.
Сопротивление активных материалов положительного и отрицательного электродов, а также сопротивление электролита изменяются в зависимости от степени заряженности аккумулятора. Кроме того, сопротивление электролита весьма существенно зависит от температуры.
Поэтому омическое сопротивление также зависит от степени заряженности батареи и температуры электролита.
Сопротивление поляризации зависит от силы разрядного (зарядного) тока и температуры и не подчиняется закону Ома.
Внутреннее сопротивление одного аккумулятора и даже аккумуляторной батареи, состоящей из нескольких последовательно соединенных аккумуляторов, незначительно и составляет в заряженном состоянии всего несколько тысячных долей Ома. Однако в процессе разряда оно существенно изменяется.
Электрическая проводимость активных масс уменьшается для положительного электрода примерно в 20 раз, а для отрицательного – в 10 раз. Электропроводность электролита также изменяется в зависимости от его плотности. При увеличении плотности электролита от 1,00 до 1,70 г./см³ его электропроводность сначала растет до его максимального значения, а затем вновь уменьшается.
По мере разряда аккумулятора плотность электролита снижается от 1,28 г./см³ до 1,09 г./см³, что приводит к снижению его электропроводности почти в 2,5 раза. В результате омическое сопротивление аккумулятора по мере разряда увеличивается. В разряженном состоянии сопротивление достигает значения, более чем в 2 раза превышающего его величину в заряженном состоянии.
Кроме состояния заряженности существенное влияние на сопротивление аккумуляторов оказывает температура. С понижением температуры удельное сопротивление электролита возрастает и при температуре -40°С становится примерно в 8 раз больше, чем при +30°С. Сопротивление сепараторов также резко возрастает с понижением температуры и в том же интервале температуры увеличивается почти в 4 раза. Это является определяющим фактором увеличения внутреннего сопротивления аккумуляторов при низких температурах.
В современных технологиях используется обратная величина, которая называется проводимостью.
Проводимость (S) = 1 / Сопротивление (R)
Ток утечки
Этот параметр присутствует в аккумуляторе любого типа. Бывает внутренним и внешним.
Внешний ток утечки определяется прежде всего качеством цепей, подключенных к батарее (отсутствием паразитных потребителей в этих цепях) и чистотой поверхности батареи.
Внутренний ток утечки невелик и для современной батареи 100Ач составляет около 1 мА (примерно эквивалентно потери 1% емкости в месяц) Его величина определяется чистотой электролита, особенно степенью загрязненности его солями металлов. [8]
Саморазряд аккумулятора
Саморазрядом называют снижение емкости аккумуляторов при разомкнутой внешней цепи, то есть при бездействии. Это явление вызвано окислительно-восстановительными процессами, самопроизвольно протекающими как на отрицательном, так и на положительном электродах. Саморазряду особенно подвержен отрицательный электрод вследствие самопроизвольного растворения свинца (отрицательной активной массы) в растворе серной кислоты. Саморазряд отрицательного электрода сопровождается выделением газообразного водорода. Скорость самопроизвольного растворения свинца существенно возрастает с повышением концентрации электролита. Повышение плотности электролита с 1,27 до 1,32 г/см³ приводит к росту скорости саморазряда отрицательного электрода на 40%. Наличие примесей различных металлов на поверхности отрицательного электрода оказывает весьма значительное влияние (каталитическое) на увеличение скорости саморастворения свинца (вследствие снижения перенапряжения выделения водорода). Практически все металлы, встречающиеся в виде примесей в аккумуляторном сырье, электролите и сепараторах, или вводимые в виде специальных добавок, способствуют повышению саморазряда. Попадая на поверхность отрицательного электрода, они облегчают условия выделения водорода. Часть примесей (соли металлов с переменной валентностью) действуют как переносчики зарядов с одного электрода на другой. В этом случае ионы металлов восстанавливаются на отрицательном электроде и окисляются на положительном (такой механизм саморазряда приписывают ионам железа). Саморазряд положительного активного материала обусловлен протеканием реакции.
2РЬО2 + 2h3SO4 -> PbSCU + 2h3O + О2
Скорость данной реакции также возрастает с ростом концентрации электролита.
Так как реакция протекает с выделением кислорода, то скорость ее в значительной степени определяется кислородным перенапряжением. Поэтому добавки, снижающие потенциал выделения кислорода (например, сурьма, кобальт, серебро), будут способствовать росту скорости реакции саморастворения двуокиси свинца. Скорость саморазряда положительного активного материала в несколько раз ниже скорости саморазряда отрицательного активного материала.
Другой причиной саморазряда положительного электрода является разность потенциалов материала токоотвода и активной массы этого электрода. Возникающий вследствие этой разности потенциалов гальванический микроэлемент превращает при протекании тока свинец токоотвода и двуокись свинца положительной активной массы в сульфат свинца. Саморазряд может возникать также, когда аккумулятор снаружи загрязнен или залит электролитом, водой или другими жидкостями, которые создают возможность разряда через электропроводную пленку, находящуюся между полюсными выводами аккумулятора или его перемычками. Этот вид саморазряда не отличается от обычного разряда очень малыми токами при замкнутой внешней цепи и легко устраним. Для этого необходимо содержать поверхность батарей в чистоте. Саморазряд батарей в значительной мере зависит от температуры электролита. С понижением температуры саморазряд уменьшается. При температуре ниже 0°С у новых батарей он практически прекращается. Поэтому хранение батарей рекомендуется в заряженном состоянии при низких температурах (до -30°С). В процессе эксплуатации саморазряд не остается постоянным и резко усиливается к концу срока службы. Снижение саморазряда возможно за счет повышения перенапряжения выделений кислорода и водорода на аккумуляторных электродах. Для этого необходимо, во-первых, использовать возможно более чистые материалы для производства аккумуляторов, уменьшать количественное содержание легирующих элементов в аккумуляторных сплавах, использовать только чистую серную кислоту и дистиллированную (или близкую к ней по чистоте при других методах очистки) воду для приготовления всех электролитов, как при производстве, так и при эксплуатации. Например, благодаря снижению содержания сурьмы в сплаве токоотводов с 5% до 2% и использованию дистиллированной воды для всех технологических электролитов, среднесуточный саморазряд снижается в 4 раза. Замена сурьмы на кальций позволяет еще больше снизить скорость саморазряда. Снижению саморазряда могут также способствовать добавки органических веществ – ингибиторов саморазряда. Применение общей крышки и скрытых межэлементных соединений в значительной степени снижает скорость саморазряда от токов утечки, так как значительно снижается вероятность гальванической связи между далеко отстоящими полюсными выводами.
Иногда саморазрядом называют быструю потерю емкости вследствие короткого замыкания внутри аккумулятора. Такое явление объясняется прямым разрядом через токопроводящие мостики, образовавшиеся между разноименными электродами.
Применение сепараторов-конвертов в необслуживаемых аккумуляторах исключает возможность образования коротких замыканий между разноименными электродами в процессе эксплуатации. Однако такая вероятность остается вследствие возможных сбоев в работе оборудования при массовом производстве. Обычно такой дефект выявляется в первые месяцы эксплуатации и батарея подлежит замене по гарантии. Обычно степень саморазряда выражают в процентах потери емкости за установленный период времени. Действующими в настоящее время стандартами саморазряд характеризуется также напряжением стартерного разряда при -18°С после испытания: бездействия в течение 21 суток при температуре +40°С. [9]
Что нужно делать для продления жизни аккумулятора автомобиля?
Каждый раз при выходе из строя аккумулятора, его владельцы думают о том, что было бы неплохо продлить жизнь АКБ. Ведь постоянные траты на покупку аккумуляторной батареи не нравятся никому. В последнее время часто встречаются случаи, когда владельцы автомобилей выбрасывают отработавший аккумулятор через 2─3 года эксплуатации. Конечно, в целом качество продукции на рынке оставляет желать лучшего, но при должном уходе жизнь среднестатистического аккумулятора должна быть примерно 5─7 лет. Как добиться такого результата и увеличить срок эксплуатации аккумулятора автомобиля.
Причины, сокращающие жизнь аккумулятора автомобиля
Все прекрасно понимают, что для долгой и нормальной работы какого-либо устройства за ним требуется регулярный уход. Это относится не только к аккумуляторным батареям, но и к любой другой технике. Производители современных аккумуляторов часто заявляют о том, что их модели не требуют обслуживания в течение всего срока жизни АКБ. Их так и называют ─ необслуживаемые.
Но для того чтобы не менять аккумулятор каждые два года, все равно нужно следить за ним и обслуживать по мере необходимости. Также важно знать причины, уменьшающие срок службы аккумулятора, и не допускать их при эксплуатации.
Срок службы аккумулятора автомобиля сильно зависит от регулярности его обслуживания. Ниже будут приведены операции, которые желательно проводить на регулярной основе.
Вернуться к содержанию
Что чаще всего сокращает срок жизни автомобильного аккумулятора?
- Испарение электролита. При эксплуатации авто, особенно в летнее время, когда под капотом особенно жарко, происходит испарение воды из электролита. В результате падает уровень электролита, и оголяются пластины аккумулятора. Это очень быстро приводит к их сульфатации;
- Аккумуляторная батарея постоянно не заряжена. Такая ситуация наблюдается при коротком характере поездок и большом количестве потребителей тока в автомобиле;
- Низкая плотность электролита. При низкой плотности электролита он может просто замёрзнуть в мороз. Это грозит тем, что пластины в банках будут покороблены. В этом случае АКБ моментально отправляется на свалку;
- Неисправная электропроводка в автомобиле. Неполадки в бортовой сети автомобиля значительно сокращают срок жизни АКБ автомобиля;
- Неаккуратная эксплуатация. Использование аккумулятора незакреплённым или плохо закреплённым может привести к ударам, опрокидыванию и т. п. В результате может быть повреждён корпус, клеммы, произойдёт замыкание.
Дополнительно можете прочитать статью про обслуживание автомобильных аккумуляторов своими руками. Вернуться к содержанию
Как увеличить срок эксплуатации АКБ?
Перечисленных выше проблем можно избежать, если регулярно осматривать аккумуляторную батарею и проводить профилактические мероприятия. Как правило, это не отнимает много времени.
Итак, что нужно делать для продления жизни аккумулятора автомобиля:
- Периодичность и процесс зарядки. Специалисты считают, что зарядка аккумулятора кардинальным образом влияет на срок службы АКБ. Аккумуляторную батарею категорически не рекомендуется держать в разряженном состоянии. Периодически нужно делать контрольно-тренировочный цикл (об этой процедуре рассказано ниже). Обязательно нужно заряжать аккумулятор после глубокого разряда (оставили фары, обогрев стекла и т. п.). Читайте также о причинах разрядки аккумулятора на автомобиле;
- Электрическая проводка авто. Бортовая сеть автомобиля должна быть исправна и содержаться в полном порядке. Особенное внимание нужно уделить генератору и регулятору напряжения в сети. Также не должно быть повреждённой проводки, окисленных или разболтанных контактов и т. п. Все эти неполадки приводят к увеличению сопротивления. В результате энергия АКБ тратиться на его преодоление и расходуется на выделение тепла. В результате сокращается срок жизни аккумулятора;
- Уровень электролита. Его нужно регулярно проверять и при необходимости корректировать. Под капотом автомобиля в процессе работы поднимается температура. В результате этого дистиллированная вода испаряется, и уровень электролита снижается. Если запустить этот процесс, то могут оголиться пластины батареи. В этом случае происходит их быстрое окисление и последующее разрушение. Обмазка с решёток осыпается и на дне образуется шлам, который иногда вызывает замыкание электродов. Все это значительно сокращает срок жизни аккумуляторной батареи. Поэтому регулярно проверяйте уровень электролита и доливайте дистиллированную воду. Уровень должен быть на 10─15 миллиметров выше свинцовых пластин;
- Поездки в зимнее время. В зимнее время года пуск двигателя затруднён из-за загустевшего масла и замёрзших свечей. Стартер крутит дольше и вытягивает из батареи больший заряд. В то же время, потребителей тока зимой мы включаем гораздо больше, чем летом. Это обогреватели стёкол, зеркал, печка, обогрев руля и сидений. Это плюс к обычным навигации и музыке. В таких условиях аккумуляторная батарея может вернуть заряд только после длительной поездки. В противном случае он будет постоянно не заряжен, что сокращает срок жизни аккумулятора. Поэтому зимой не рекомендуются кратковременные поездки (завелись, проехали 5 минут до магазина, снова завелись и немного проехали обратно);
- Профилактика коррозии клемм. Следите за состоянием клемм аккумулятора. На них не должно быть налёта белого цвета (окислы). Если появились следы окисления, то снимите аккумулятор, промойте клеммы раствором пищевой соды и высушите. Если следы коррозии сильные, то можно обработать их наждачной бумагой. Клеммы должны быть хорошо затянуты, желательно покрыть их специальным составом для контактов. Он продаётся в автомобильных магазинах и стоит недорого;
- Плотность электролита. Плотность полностью заряженной батареи составляет 1,27 гр./куб. см. Рекомендуем проверять это значение через некоторое время после полной зарядки АКБ. Низкая плотность электролита может привести к серьёзным проблемам зимой. Электролит просто замёрзнет. По ссылке можно посмотреть таблицу плотности электролита и связанных с ней характеристик;
- Чистота АКБ. Кому-то это покажется странным, но грязь тоже сокращает срок жизни аккумулятора. Грязь, пыль, подтеки электролита на поверхности АКБ превращаются в проводящий слой, который вызывает разряд батареи и снижение ёмкости. Поэтому хотя бы верхняя плоскость аккумулятора должна быть чистой и сухой. Если позволяет подкапотное пространство, можно сделать некое подобие крышки для АКБ, чтобы на поверхность и клеммы не попадала влага, пыль, масло;
- Периодический осмотр. Для продления срока эксплуатации желательно делать периодический визуальный осмотр аккумулятора. Например, когда проверяете уровень масла в двигателе и охлаждающей жидкости в расширительном бачке, заодно проводите осмотр АКБ. Это позволит своевременно выявлять повреждения корпуса, следы окисления на клеммах, загрязнения аккумулятора;
- При простое автомобиля. Если вы оставляете автомобиль на длительное хранение, то АКБ с него лучше снять, полностью зарядить и хранить отдельно. Это продлит жизнь батареи.

Периодически заряжайте аккумулятор
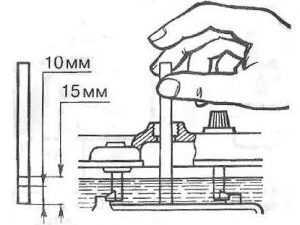
Проверяйте уровень электролита
Содержите аккумулятор в чистоте
Вернуться к содержанию
Контрольно-тренировочный цикл
Выше говорилось о необходимости периодически проводить контрольно-тренировочный цикл (КТЦ) для аккумулятора. Опытные специалисты говорят, что для продления срока жизни АКБ эту процедуру необходимо проводить раз в год. В чём же она заключается?
Такой цикл включает в себя полную зарядку, контролируемый разряд аккумулятора. После этого батарея снова полностью заряжается. Перед проведением КТЦ аккумулятор снимается с автомобиля. Проводится полная зарядка, после которой замеряется плотность электролита. Для этого существует ареометр. Стоимость в магазинах около 100 рублей. Требуемое значение 1,27 гр./куб. см. Если плотность выше этого значения, то в банки доливают дистиллированную воду, а когда ниже – готовый электролит (предварительно нужно выбрать старый).
После полной зарядки проводится контролируемый разряд. Для этого собирается схема разрядного устройства.
Для этого потребуется реостат с сопротивлением 4─6 Ом, а также амперметр и вольтметр для контроля процесса разрядки. Процесс разрядки проводится, в так называемом 10 часовом режиме. В этом случае ток устанавливается, как 9 процентов от ёмкости батареи. К примеру, для аккумулятора 62 А-ч это значение составит примерно 5,6 ампер. Этот ток разряда нужно поддерживать до тех пор, пока напряжение на аккумуляторе не упадёт до 10,3 вольт. Дальнейшее снижение напряжения не рекомендуется. Если замерить время падения напряжения до 10,3 вольт и умножить его на ток разряда, то вы получите реальную ёмкость вашего аккумулятора. Если нет возможности собрать разрядное устройство, можно просто параллельно подключить к АКБ автомобильную лампочку подходящей мощности, а ток и напряжение контролировать при помощи мультиметра.
После разряда аккумулятора, сразу ставьте его на зарядку. Ток зарядки при этом должен быть не выше 10 процентов от номинальной ёмкости аккумулятора. В процессе зарядки напряжение на клеммах АКБ не должно превышать 15,5─16 вольт. Некоторые опытные аккумуляторщики рекомендуют заряжать аккумулятор 12 часов током 10 процентов от номинальной ёмкости, а затем снизить в два раза и оставить ещё на 12 часов. Так, батарея наберёт максимальную ёмкость. Если регулярно проводить такой контрольно-тренировочный цикл, то можно существенно продлить жизнь автомобильному аккумулятору. Здесь стоит отметить, что такой цикл не рекомендуется делать для кальциевых АКБ. Для них глубокий разряд не рекомендуется. Несколько таких разрядов и их можно отправлять на утилизацию аккумуляторных батарей. Если вас беспокоит вопрос, а нужно ли заряжать новый автомобильный аккумулятор после покупки, можете прочитать статью по указанной ссылке. Вернуться к содержанию
Обслуживать или платить?
Как видите, ничего особенно сложного в регулярном обслуживании аккумулятора нет. По крайне мере, визуально контролировать состояние аккумулятора и уровень электролита может каждый. В случае отклонения от нормы можно обратиться к специалистам за помощью на ранней стадии какой-то проблемы, а не в запущенном состоянии.
В этом случае реально продлить срок жизни аккумулятора до 5─7 лет. Если же у достаточно средств, чтобы менять аккумулятор, как расходник типа масла и фильтров, то можете не «заморачиваться» с обслуживанием. Тогда срок жизни аккумулятора автомобиля составит 2─3 года. Снимите старый, поставите новый и поедете дальше.
Вернуться к содержанию
Заряд-разряд аккумулятора
Электрический аккумулятор (аккумуляторная батарея, АКБ) – одно из важнейших изобретений человечества в начале 19 века, созданное для обеспечения автономного электропитания различных устройств. Применяется на сегодняшний день во многих сферах деятельности, но наиболее широкое распространение получило его использование в автомобилях.
Автомобильный аккумулятор является источником электрического тока многоразового действия, то есть с помощью процесса «заряд-разряд» можно использовать АКБ довольно долгое время. Процесс заряд-разряда представляет собой доведение аккумуляторной батареи до состояния разряда во время ее использования, а затем до состояния полного заряда, достигаемого за счет зарядного устройства.
В аккумуляторе есть несколько активных веществ – свинец и электролит – с помощью которых и хранится заряд. Если же АКБ разряжена полностью, то спустя некоторое время в ней произойдет процесс сульфатации – снижение плотности электролита и образование сульфата свинца, препятствующего заряду аккумулятора. Так что хранить длительное время разряженную батарею не рекомендуется.
Специальные зарядные устройства с функцией десульфатации
Существуют специальные зарядные устройства с функцией десульфатации, позволяющей растворить сульфат свинца с помощью импульсов реверсивного тока или тренировочных циклов. Такие методы либо восстановят работоспособность устройства, либо позволят установить, что аккумулятор полностью непригоден к эксплуатации.
Метод реверсивного тока предполагает заряд АКБ малыми реверсивными токами, замене электролита и залива дистиллированной воды в процессе восстановления. Тренировочный цикл представляет собой следующий процесс: полный заряд АКБ номинальным током, трехчасовое ожидание, перемешивание электролита путем получасового заряда, контрольный десятичасовой разряд аккумулятора, полный разряд, полный заряд.
Подытожив, можно сказать, что заряд аккумуляторной батареи можно восстановить практически в любых случаях, за исключением очень глубокой сульфатации. Главное, что нужно сделать, это купить правильное зарядно-разрядное устройство, которое имеет функцию десульфатации и соблюдать рекомендации при проведении заряда. Примером такого устройства является десульфатирующее зарядно-разрядное устройство ЗЕВС производства нашей компании. Для более подробного ознакомления с ним пройдите по ссылке.
Рекомендуем ознакомиться со следующими материалами:
"Питер - АТ"
ИНН 780703320484
ОГРНИП 313784720500453