Принцип работы батарейки
Как устроена батарейка? Принципы работы батарейки
Всего просмотров: 4 756Просмотров за сутки: 0Если верить археологам, то первые батарейки появились еще 2000 лет назад. Во время раскопок в Ираке нашли глиняную вазу, залитую битумом, в который были вделаны медный и железный стержень. Действительно ли это использовалось в качестве источника электричества, трудно сказать — это всего лишь предположения.
Первой современной батарейкой по праву можно назвать «Вольтов столб» — устройство, созданное итальянским физиком Алессандро Вольта в 1800 году.
 Алессандро Вольта
Алессандро Вольта «Вольтов столб» представлял собой стопку из пластин разных металлов — цинковых и медных. Между ними клалась ткань, смоченная в кислоте. Химическая реакция между элементами «Вольтова столба» создавала электричество.
Вольтов столбЕго работа основывалась на предположениях Луиджи Гальвани, который проводил опыты с лягушкой, подводя к ее лапке металлические полоски.
 Луиджи Гальвани
Луиджи Гальвани Однако, Л. Гальвани сделал неправильные выводы, решив, что само животное обладает электричеством, назвав это «животным электричеством». А. Вольта правильно понял, что разряд возникал из-за того, что лапка, находившаяся между двумя полосками металла, была влажной и служила в качестве проводника.
По имени Л. Гальвани «Вольтов столб» и другие источники электричества подобного типа получили название «Элемента Гальвани» или «Гальванического элемента». Это, на самом деле, более правильное название для таких устройств, так как батарейка — это батарея, т.е. серия гальванических элементов, соединенных между собой. А единицу напряжения, которую давал гальванический элемент, назвали «вольтом» в честь Алессандро Вольта.
Принцип работы батарейки
Во многом принцип работы батарейки тот же, что и в изобретении Вольта, несмотря на технологический прогресс в их изготовлении. Любая батарейка устроена схожим образом, в ней обязательны три элемента, между которыми происходит химическая реакция, в результате которой возникает электричество: электроды — анод, катод, и электролит.
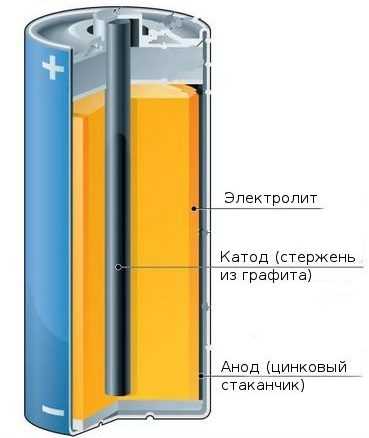 Устройство батарейки
Устройство батарейки Все эти элементы присутствовали изначально и в «Вольтовом столбе». В качестве анода, который является источником электронов, выступает чаще всего цинк. Электролит — как правило, специальное вещество (соль, щелочь), через которое осуществляется взаимодействие электродов между собой. Анод обозначается как «-» (минус), а катод — как «+» (плюс).
Какие бывают батарейки?
Батарейки бывают, в основном, солевыми и щелочными. Жидкие электролиты в них не используются, их определенным образом сгущают, например, при помощи крахмала.
Солевые батарейки, изобретенные в 1865 году — наиболее дешевые в изготовлении, для их производства используют уголь, цинк и хлорид аммония (в качестве электролита). Помимо простоты изготовления и дешевизны, имеют такие недостатки, как окисление, засоливание цинковой оболочки, что приводит солевую батарейку в негодность.
Щелочные батарейки имеют маркировку Alkaline, хранятся они дольше и дают более стабильное напряжение.
 Щелочные батарейки
Щелочные батарейки В принципе, это те же солевые батарейки, однако, разница между солевыми и щелочными батарейками заключается в том, что элементы в них расположены в обратном порядке, а цинк находится в порошкообразном состоянии, что увеличивает контакт элементов батареи между собой, делает их более надежными. Щелочные батарейки имеют гораздо больший объем заряда, что позволяет их использовать в энергоемких приборах (цифровых фотоаппаратах, фонариках, электронные игрушки с электродвигателями и т.п.). Они долговечны, лучше справляются с работой при низких температурах.
Наиболее современны литиевые батарейки (литий входит в состав анода), которые долговечны и безопасны в работе однако, дороже в производстве.
 Литиевые батарейки
Литиевые батарейки К их преимуществам по сравнению с щелочными можно отнести возможность создавать максимально плоские батареи, изготавливать батареи с большим количеством вариантов напряжения, долговечность — в некоторых приборах они могут работать до 15 лет! Их используют в наручных часах, калькуляторах, памяти системной платы компьютера и других приборах.
Проблема всех батареек — необратимость химических реакций. При использовании или с течением времени анод разрушается, либо покрывается продуктами окисления и перестает работать. В таких случаях мы говорим, что батарейка села. Но прогресс не стоит на месте — оказалось, что соединив определенным образом вещества, входящие в состав батареи, можно, пропустив ток через нее, вернуть в прежнее состояние. Такие батареи назвали аккумуляторами — работа батареи в них восстанавливается посредством пропускания электричества в обратном направлении, от катода к аноду. А сам процесс мы все знаем, как «зарядку», т.е. батарея «заряжается». Обычные батареи, рассмотренные выше, заряжать, конечно, нельзя, они для этого не приспособлены — это может привести к их течи или взрыву.
Оцените прочитанное: (8 оценок, среднее: 5,00 из 5) Загрузка...Принцип работы батарейки
03.09.2018
Принцип работы батарейки заключается в простой химической реакции, которая происходит обычно между тремя элементами. В результате, реагирования веществ между собой, получается электрический ток. Это если говорить кратко.
Три ключевых объекта:
- Анод «+»
- Катод «-«
- Электролит
Анод или положительный полюс служит источником электронов. Обычно его изготавливают из цинка. Два электрода заставляет взаимодействовать между собой электролит. В качестве электролита выступает обычно соль, хлорид аммония или щелочь. Он может быть в сухом и жидком виде. Чтобы сделать густым это вещество производители добавляют полимерные соединения. Некоторые используют крахмал.
Принцип действия батарейки
Ток поступает с положительного полюса на отрицательный. Это происходит если к батареи подключена нагрузка. Если просто соединить плюс и минус проводом произойдет замыкание. В результате этого может быстро сесть батарейка, а также произойти возгорание.
Катод играет роль восстановителя. Он приобретает электроны от анода. В электролитной среде ионы прекрасно передвигаются и способствуют хорошей выработке тока.
Что происходит с точки зрения химии?
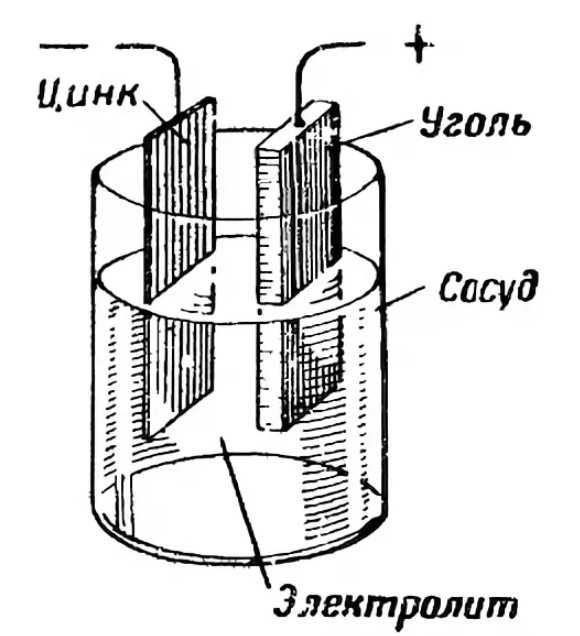
К примеру, в стеклянную емкость нальем раствор серной кислоты и поместим туда стержень, выполненный из цинка. На поверхности данного стержня имеются положительно заряженные ионы. А вокруг этого цинкового объекта, в растворе, скапливаются отрицательные ионы вещества. У раствора имеются силы притяжения, которые с легкостью отрывают ионы цинка. В результате жидкость получает положительный заряд, а цинковая пластина или стержень отрицательный. Из физики известно, что разность потенциалов равна напряжению. Отсюда и возникает электрический ток.
В итоге, когда происходит контакт кислотного раствора и металла на границе образуется электрическое поле. В момент его появления химическая энергия превращается в электрическую. Таков принцип работы батареи.
Через некоторое время ресурс батареи будет истощен. Все зависит от того где и как используется источник питания. Например, если от него работает фонарик, то при умеренном использовании 2-х батарей на 1,5 вольта каждая, хватит на 1 месяц. Но если вставить эти же самые батарейки в электрическую машинку, она будет работать несколько часов.
В результате всего этого можно сделать вывод что чем больше нагрузка, тем быстрее разрядиться батарейка.
Читайте так же:
Устройство батарейки
Читайте так же
Принцип работы батарейки Ссылка на основную публикациюУстройство батарейки: из чего состоит, принцип работы
Устройство батарейки несложное, но без нее трудно представить современную жизнь. Она применяется повсеместно во многих бытовых приборах. С данными источниками питания знакомы даже маленькие дети, ведь все электронные игрушки работают от них. А вот как работает батарейка и из чего она сделана, знают далеко не все.
Что ж, давайте рассмотрим принцип работы обычной батарейки.
Содержание
- 1 Краткое описание
- 2 Принцип работы
- 3 Какими бывают батарейки
Краткое описание
Прежде чем разбираться, из чего состоит батарейка, выясним, что это такое. Батарейка – это наипростейшее устройство для получения электричества, которое представляет собой гальванический элемент. Суть работы элемента составляет метод, основанный на химическом взаимодействии одних веществ с другими.

Изобретателем считается ученый Алессандро Вольта. Но есть данные, которые свидетельствуют о том, что гальванические устройства появились задолго до того, как их разработал физик.
Теперь можно приступить к знакомству с тем, как устроена привычная всем нам батарейка.
Принцип работы
На прилавках магазинов представлено множество различных видов батареек. У них есть небольшие различия, но вот работают они все по одной схеме. Если есть старая батарейка, сделайте ее разбор, и вы увидите, какова ее анатомия.
Каждая из них имеет в своем строении несколько элементов, состоящих из:
- положительного полюса – анода (цинк);
- отрицательного полюса – катода (марганец);
- электролита – сухого или жидкого.
Вот эти три компонента батарейки и определяют ее состав.
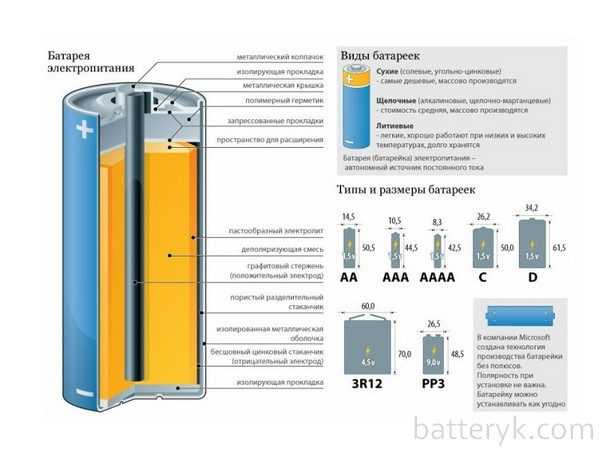
Принцип работы устройства такой: происходит поступление электрического тока с положительного заряда (анода) на отрицательный (катод). При этом важно помнить, что необходимо присутствие нагрузки: лампочки, двигателя, диода или какого-либо иного элемента. Отсутствие нагрузки во время соединения «плюса» с «минусом» грозит коротким замыканием.
Катоды выступают восстановителем. Они получают электроны от поступившего анода. Электролит представляет собой среду для передвижения ионов, образовавшихся в результате химических реакций.
В процессе эксплуатации аккумуляторов постоянно образуются определенные вещества, аноды же в ходе работы элемента приходят в негодность, разрушаются, окисляются. Таким образом источник питания садится.
Многих интересует вопрос: «А возможно ли его заряжать?» Все, что происходит в батарейках – необратимо. Поэтому гальванические элементы не заряжаются. Но с помощью достижений науки есть возможность возвратить изначальное состояние элементам. Для этого необходимо пропустить электрический ток в противоположную сторону, то есть от катода к аноду. Такие источники питания получили название аккумулятора, а сам процесс мы видим на примере обычной зарядки.

Но вот традиционные устройства с помощью этой рецептуры зарядить нельзя. Они не подходят для повторного использования, так как это чревато взрывом или течью химических элементов из корпуса.
Какими бывают батарейки
Существует несколько типов элементов. В большинстве своем они солевые или щелочные. Жидкими не пользуются, потому что при переворачивании они выходят из строя. Слишком текучий электролит загущают.
Батарейки, в зависимости от состава, могут быть таких видов:
Помимо специфического состава, эти источники тока отличаются своими параметрами и объемом заряда.
Теперь вы знаете, каким характеристикам соответствует работа гальванического элемента. Если хотите все увидеть наглядно, разберите старую батарейку из сухих элементов и изучите ее устройство.
Батарейка и всё о ней
 Батарейка — это слово плотно вошло в нашу повседневную жизнь. Но, к сожалению, сегодня мало кого интересует её история, устройство, её виды. Давайте вместе разберёмся с этими и другими интересными вопросами о батарейке. А точнее «что такое батарейка», «как работает батарейка». Повседневная жизнь не требует каких-то великих усилий для включения телевизора, калькулятора, для нормальной работы настенных часов, для работы компьютерной мыши и так далее. А все благодаря каким-то батарейкам, которые помогают упростить нашу жизнь, помогают сэкономить наше время. Это понимает каждый здравомыслящий человек, но не каждый задаёт себе вопрос: «как из таких маленьких батареек совершается такой объём работы», «как устроены батарейки»… А, между тем, это физика.
Батарейка — это слово плотно вошло в нашу повседневную жизнь. Но, к сожалению, сегодня мало кого интересует её история, устройство, её виды. Давайте вместе разберёмся с этими и другими интересными вопросами о батарейке. А точнее «что такое батарейка», «как работает батарейка». Повседневная жизнь не требует каких-то великих усилий для включения телевизора, калькулятора, для нормальной работы настенных часов, для работы компьютерной мыши и так далее. А все благодаря каким-то батарейкам, которые помогают упростить нашу жизнь, помогают сэкономить наше время. Это понимает каждый здравомыслящий человек, но не каждый задаёт себе вопрос: «как из таких маленьких батареек совершается такой объём работы», «как устроены батарейки»… А, между тем, это физика.
Самые первые прототипы батареек появились ещё в Месопотамии около 2000 лет назад. Состояла она в то время из глиняной вазы, медного и железного стержней, залитыми битумом. Кстати, если такой сосуд залить кислотой (уксусной, серной), то получим напряжение примерно в 1В. Назвали такой прототип «Багдадской батарейкой » в связи с местом, на котором были обнаружены. Примерно в 1800 году итальянский физик Алессандро Вольта изобрёл батарейку, которой мы и по сей день продолжаем пользоваться. Кстати, кто не знает что такое батарейка, так это источник питания, который вырабатывает электричество под действием химического процесса. То есть батарейка это гальванический элемент, работающий на химической реакции. Так можно объяснить и детям.
____________________________________________
Возможно, вам будет интересно: Почему батарейки кислые на вкус?
__________________________________________________________________
Как работает батарейка
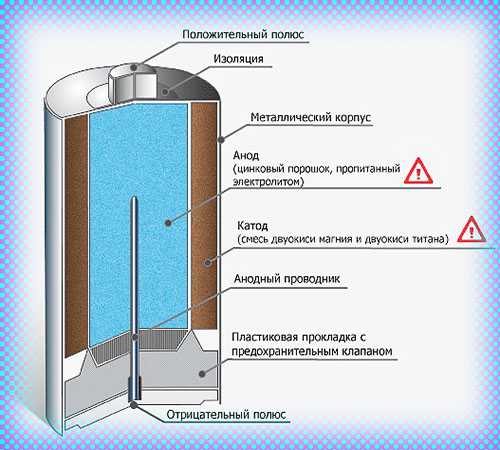 Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким), именно эти элементы и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.). Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится. Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит. Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким), именно эти элементы и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.). Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится. Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит. Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Виды батареек
- Солевые (угольно-цинковые, марганцево-цинковые) батарейки.
Изготовляются из пассивного угля и двуокиси марганца, электролит из хлорида аммония и катод из цинка. В перерывах работы элементы питания могут восстанавливаться, т.е. выравнивать локальные неоднородности в композите электролита, вызванных разрядом. Такой процесс немного продлевает срок службы батарейки.
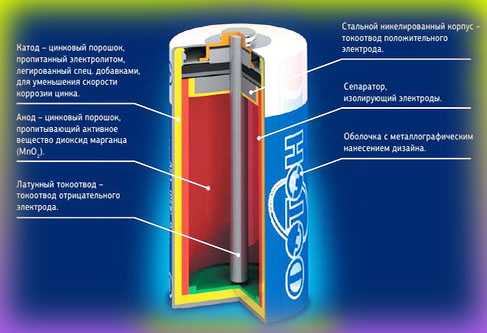
- Алкалиновые (щёлочные) батарейки
В отличие от солевых батареек у этих химический элемент электролита — щелочной электролит. Щёлочные батарейки (алкалин) имеют продолжительный срок хранения, а в процессе эксплуатации напряжение на электродах меняется гораздо меньше, чем у элементов с солевым раствором.
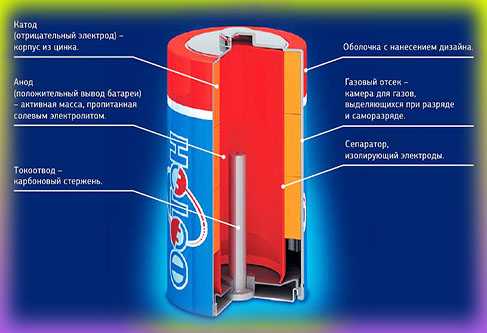
- Литиевые батарейки — li ion
Самые современные. В отличие от щёлочных и солевых батареек, в состав катода входит литий (Li – наивысший отрицательный потенциал), в состав анода — различные материалы. Электролит — органический электролит. В связи с такими элементами литиевые батарейки получили большой срок хранения, большую плотность энергии и различную рабочую температуру.
что такое батарейка АА
Что такое батарейка типа АА — пальчиковые.
Что такое батарейка ААА — мизинчиковые (те, что мы привыкли использовать в пультах).
"Питер - АТ"
ИНН 780703320484
ОГРНИП 313784720500453